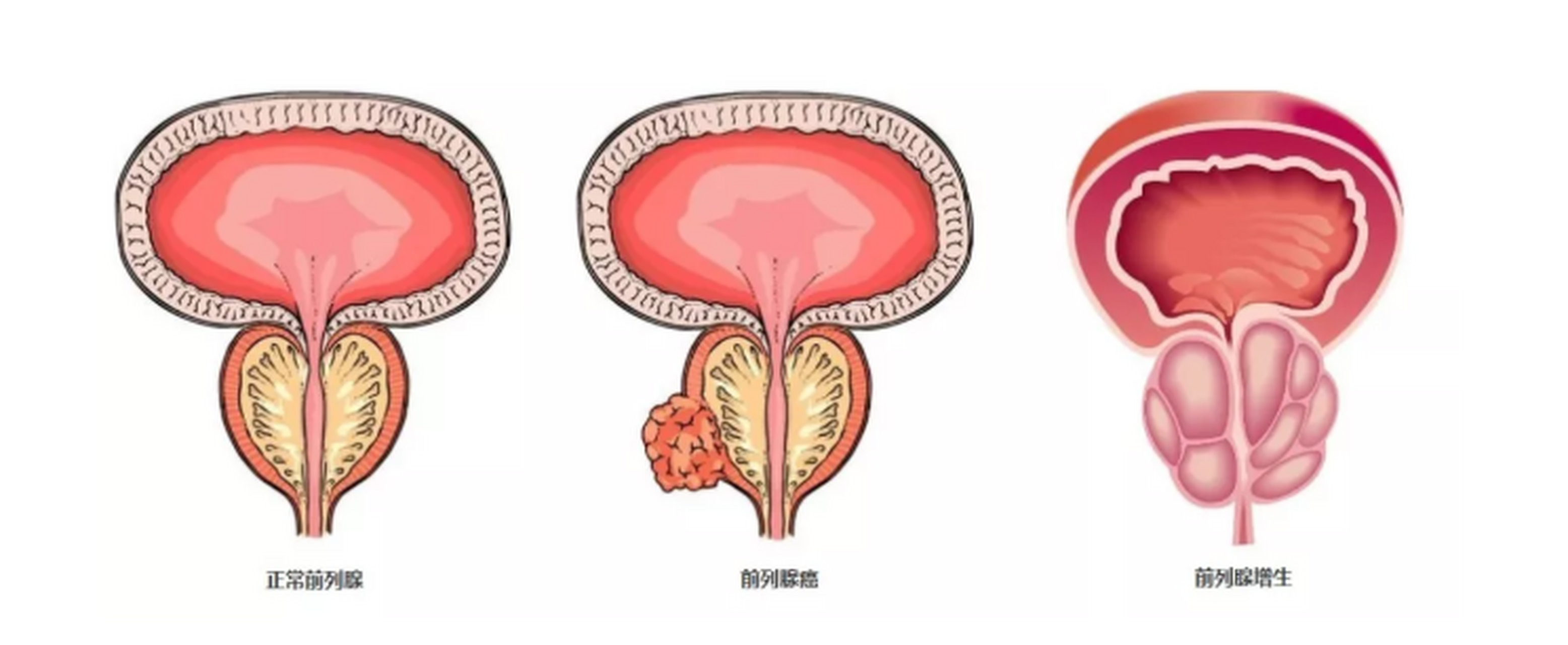
培米替尼(Pemigatinib)能用于尿路上皮癌吗?
FGFR突变发生在大约7%的癌症中,尤其常见于尿路上皮癌和胆管癌。大约50%的膀胱癌具有FGFR基因改变;75%的NMIBC和大约15%的高级别侵袭性尿路上皮癌携带FGFR3基因改变,2%的尿路上皮癌症携带FGFR2突变。与尿路上皮癌不同,胆管癌表现出FGFR2融合或重排的高比率。在高达11-45%的诊断为iCCA的患者中发现了FGFR2融合,这可能与良好的预后有关。最近对FGFR抑制剂的临床前研究支持这些基因改变作为治疗靶点的潜力。几种FGFR抑制剂在伴有FGFR2和FGFR3改变的胆管癌和癌症尿路上皮癌中表现出活性。
在尿路上皮癌中,以顺铂为基础的一线化疗后,OS可达到14-15个月。以埃达非替尼作为二线治疗,观察到mPFS为5.5个月,mOS为13.8个月。Pemiginib是美国食品药品监督管理局(FDA)批准的第一种用于胆管癌FGFR2融合的FGFR抑制剂。最近,因福替尼和福替巴替尼也获得了FDA对这种癌症的批准。埃达非替尼被批准为携带FGFR2/3融合或突变体的尿路上皮肿瘤的一线治疗,以及转移性或不可切除的尿路内皮癌的二线治疗。这些令人鼓舞的结果有望在携带FGFR的肿瘤的一线治疗中应用FGFR抑制剂。

培米替尼(Pemigatinib)能用于尿路上皮癌吗?
Pemiginib是一种选择性FGFR1-3抑制剂,已被美国食品药品监督管理局批准用于先前接受系统治疗的患者,这些患者被诊断为患有FGFR2融合或其他重排的不可切除、局部晚期或转移性胆管癌。
FIGHT-202(NCT02924376)的II期临床试验证明,在被诊断为晚期/转移性胆管癌和FGFR2融合或重排的患者(n=108)中,作为二线或后二线治疗的培咪嗪尼的客观有效率(ORR)为37.0%(95%CI,27.9-46.9)。中位反应持续时间(mDOR)为8.1个月(95%CI,5.7-13.1)。mPFS为7个月(95%CI,6.1–10.5),中位总生存期(mOS)为17.5个月(95%CI,14.4–22.9),疾病控制率(DCR)为82.4%(95%CI为73.9–89.1)。
尽管这些患者对培咪嗪尼有这些令人印象深刻的反应,但携带FGFR扩增或突变的患者的结果令人失望。进行了另一项II期研究(NCT04256980),以评估在系统治疗中取得进展的晚期或转移性胆管癌合并FGFR2融合或重排患者(n=30)中使用培咪嗪尼的情况。该研究证明ORR为50%(95%置信区间,31.3-68.7),DCR为100%(95%可信区间,88.4-100),mPFS为6.3个月(95%置信度,4.9-不可估计)。这两项研究都没有对照组,因此很难评估培伐替尼的相对有效性。III期研究FIGHT-302(NCT03656536)比较了培伐替尼与吉西他滨加顺铂化疗在不可切除或转移性胆管癌中的疗效和安全性。另一项研究是一项I期试验(NCT04088188),正在评估培伐替尼与吉西他滨和顺铂联合使用的疗效。
Pemiginib也在招募尿路上皮癌患者的试验中进行了研究。进行了一项II期研究FIGHT-201(NCT02872714),以评估在系统治疗后进展为FGFR3突变或融合的转移性或手术不可切除的尿路上皮癌患者(n=64)中使用培咪嗪尼的情况。ORR达到25%(95%CI,14-40),mPFS为4.1个月。然而,培伐替尼对这些患者的长期疗效和潜在生存益处尚未确定。另一项二期研究PEGASUS(NCT04294277)评估了接受根治性手术的高危尿路上皮癌症患者中的培咪嗪尼。最后,一项II期研究(NCT03914794)目前正在招募尿路上皮癌患者,以评估培伐替尼的疗效。
免责声明
由本文所表达的任何关于疾病的建议都不应该被视为医生的建议或替代品,请咨询您的治疗医生了解更多细节。本站信息仅供参考,医康行不承担任何责任。

扫码实时看更多精彩文章
